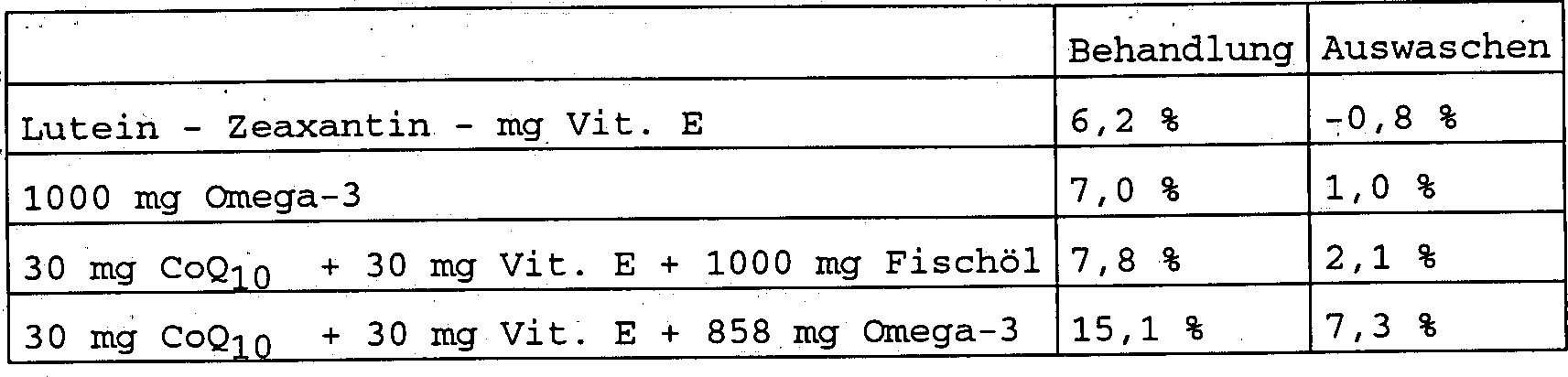-
Diese Erfindung betrifft eine pharmazeuti
sche/Nährstoffzusammensetzung,
zur Verwendung bei der Unterstützung
und/oder Schaffung einer Therapie für Individuen mit einem Risiko
und/oder mit einer Behandlung für
Disfunktionen des Energiemetabolismus und spezifisch für mitochondriale
Erkrankungen.
-
Mehr spezifisch betrifft diese Erfindung
eine Zusammensetzung, umfassend (a) eine Menge eines Lipid-löslichen
Benzochinons, ausgewählt
aus der Gruppe, bestehend aus Ubichinon (Coenzyme Q10 CoQ10) seine reduzierte Form, Ubichinol-10 (CoQ10H2) oder Mischungen
davon, die wirksam ist zur Erzeugung einer therapeutischen und/oder
vorbeugenden und/oder Nährstoff-Aktivität und (b)
zumindest eine weitere Komponente, die zur Stimulierung und Verstärkung des
intramitochondrialen Transportes der Komponete (a) geeignet ist,
zur Erzeugung eines Medikamentes zur Vorbeugung und/oder Behandlung
von Mitochondriopathien.
-
Demgemäß kann die Zusammensetzung
die Form einer Diät-
oder Nähr
stoffergänzung
oder einer tatsächlichen
Medizin einnehmen und diese Wirkung ausüben in Abhängigkeit vom Träger oder
der Vorbeugungswirkung oder der strikt therapeutischen Wirkung,
die die Zusammensetzung in Bezug auf die bestimmten Individuen ausüben soll,
die diese verwenden. In Abhängigkeit
von den tatsächlichen
Umständen
muss die Zusammensetzung zur Verwendung gemäß dieser Erfindung nicht unbedingt
unter der Aufsicht eines begleitenden Arztes angenommen werden,
kann aber alternativ so erfolgen.
-
Die folgende Definition wird gegeben,
was eine mitrochondriale Erkrankung ist und was die triggernde, sub-zellulären Ursachen
sind:
-
"Die Mitochondrien erzeugen Adenosintriphosphat
(ATP), die mobile Körperenergiequelle.
Wenn Mutationen auftreten, die die Mitochondrien beeinflussen, wird
die vitale Zufuhr von ATP unterbrochen, immer weniger Energie wird
innerhalb der Zelle erzeugt. Wenn dieses Verfahren im Körper in
großem
Umfang wiederholt wird, misslingt das gesamte System, und das Leben
der Person, bei der dieses auftritt, kann gefährdet, geändert oder sogar beendet werden.
Die Zellen, die die meiste Energie erfordern, wie das Gehirn, Herz
und die Skelettmuskeln, sind am stärksten verwundbar."
-
Eine detaillierte Liste und Beschreibung
der mitochondrialen Er krankungen wird angegeben, die unter anderem
Coenzym Q10 Mangel, Komplex III Mangel (Ubichinon-Cytochrom
c Oxidoreduktasemangel), dessen Symptome pigmentäre Retinopathie umfassen; Komplex
IV Mangel/COX-Mangel (Cytochrom-c-Oxidasemangel), dessen Symptome
optische Atrophie und Ophthalmoplegie umfassen; CPEO (chronisches
progressives externes Ophthalmoplegie-Syndrom), dessen Symptome visuelle Myopathie
und Retinis pigmentosa umfassen; ARMD (alterbezogene makulare Degenerierung);
NARP (Neuropathie, Ataxie und Retinis pigmentosa) und viele andere
umfassen.
-
Weil CoQ10 für zelluläre Bioenergetiken
unverzichtbar ist, kann sein Mangel einen Wirt für Pathologien vergeben.
-
Tatsächlich ist bekannt, dass CoQ10 eine essentielle Rolle als Elektronen(Redox)-Träger in der
mitochondrialen Elektronentransportkette der Zelle spielt. Jedoch
schützt
es ebenfalls die Membranphospholipide und solche in LDL vor der
Peroxidation und schützt
ebenfalls Vitamin E oder regeneriert es. CoQ10 wird
im Körper
von Vorläufern
der Cholesterinsynthese synthetisiert und wird daher nicht als ein
Vitamin klassifiziert. Jedoch vermindert sich die Fähigkeit
zur Synthese von CoQ10 mit dem Alter und
es kann eine zunehmende Abhängigkeit
von der Nahrung für
die Zufuhr des Nährstoffes
sein. Die am reichlichsten vorhandenen Quellen sind frische unverarbeitete
Nahrungsmittel, insbesondere Fleisch, Fisch, Nüsse und Samenöle. Die
durchschnittliche tägliche
Aufnahme von CoQ10 ist ungefähr 2 mg.
-
Ubichinol-10 oder CoQ10-H2, die reduzierte Form von CoQ10 spielt
eine zweite Rolle als starkes lipidlösliches Antioxidans, und seine
Aktivität
bei physiologischen Konzentrationen in den Lipidkomponenten von Zellen
wurde vor kurzem gezeigt.
-
Der antioxidative Elektronentransport
von CoQ10 und die Membranstabilisierenden
Eigenschaften wurden in großem
Umfang untersucht, mit dem Ziel, verschiedene kardiovaskuläre Erkrankungen,
einschließlich die
Verhinderung der zellulären
Schädigung
während
der Reperfusion, Angina pectoris, Hypertonie, Myocardischämie und
kongestiver Herzinsuffizienz vorzubereiten und/oder zu behandeln.
-
Bei Patienten mit mitochondrialer
Enzephalomyopathie erhöht
die CoQ10 Behandlung die mitochondrialen
Funktionen und Bewegungsleistung und vermindert die Azidose, die
mit der Bewegung assoziiert ist. Diese Feststellung ist mit der
CoQ10 Teilnahme beim Elektronentransport
und den mitochondrialen Membranen und der biologischen Oxidation
von Zellbrennstoffen für
die Energieerzeugung konsistent.
-
Es wurde ebenfalls berichtet, dass
ein CoQ10 -Mangel mit Viralinfektionen assoziiert
ist, und die Ergänzung
von CoQ10 bei Patienten mit einem erworbenen
Immunmangelsyndrom (AIDS) führte
zu einer verstärkten Makrophatenaktivität und einem
erhöhten
Serumgehalt von IgG. Es wurde berichtet, dass eine CoQ10 -Behandlung
einige Vorteile bei Krebspatienten und eine verstärkte hämatopoetische
Aktivität
bei schlecht ernährten
Kindern bringt. All diese Beweise legen nahe, dass CoQ10 essentielle
Rollen bei der Aufrechterhaltung und der Förderung der Gesundheit unter
normalen und abnormalen Bedingungen spielen kann.
-
Es ist zunehmend mehr ersichtlich,
dass Individuen mit einem Risiko und/oder mit einer Behandlung bezüglich der
Mitochondriopathien eine verstärkte
Ergänzung
von Ubichinonen in Bezug auf die normale Aufnahme dieser Substanzen
durch die Diät
erfordern, weil insbesondere der CoQ10 Mangel
den Beginn, das Auftreten oder die Verschlimmerung der Symptome
einer ernsthaften Mitochondriopathie verursachen können.
-
Viele Versuche wurden während der
letzten Dekade durchgeführt,
um Formulierungen zu finden, die die Bioverfügbarkeit von CoQ10 oder
irgendwie seine Wirksamkeit bei den zellulären Organellenstellen der Wirkung
verstärken.
Zum Beispiel berichten M. Weis et al in "Bioavailability of four
oral Coenzyme Q10 formulations in healthy
volunteers (Molec. Aspects Med. Bd. 15 (Ergänzung) S. 273-s, 280, 1994) über einen
4-Wege-Zufalls-Mehrfachaustauschversuch,
worin die Bioverfügbarkeit
von vier verschiedenen CoQ10-Formulierungen verglichen
wurde. Die Untersuchungsergebnisse legen nahe, dass eine Sojabohnenölsuspension
von CoQ10 (Bioquinon® 100
mg CoQ10 mit 400 mg Sojabohnenöl in weichen
Gelatinekapseln) die höchste
Bioverfügbarkeit
entfaltet.
-
Trotz all dieser Wirkungen wurden
bisher jedoch keine zufriedenstellenden Formulierungen entwickelt, die
in der Lage sind, eine therapeutische oder vorbeugende wirksame
Konzentration von Ubichinonen und insbesondere CoQ10 an
ihren intrazellulären
Stellen der Wirkung zu schaffen.
-
Polyungesättigte Fettsäuren (PUFA)
sind in Klassen unterteilt, die auf der Lokalisierung der ersten Doppelbindung
basieren, wenn von dem Methylende des Fettsäuremoleküls gezählt wird: ω-3 (oder n-3) Fettsäuren haben
die erste Doppelbindung zwischen dem dritten und dem vierten Kohlenstoffatom,
und die ω-6 (oder
n-6)-Fettsäuren
haben ihre erste Doppelbindung zwischen dem sechsten und dem siebten
Kohlenstoffatom. Besonders wichtig sind die ω-3 Fettsäuren und spezifisch Linolensäure (18
: 3 ω3)
(LNA), Eicosapentaensäure
(20 : 5 ω3)
(EPA) und Docosahexaensäure
(22 : 6 ω3)
(DHA), worin die erste Zahl (vor dem Doppelpunkt) die Zahl der Kohlenstoffatome
im Molekül
und die zweite Zahl die Anzahl der Doppelbindungen angibt.
-
In den letzten beiden Dekaden haben
epidemiologische Studien, klinische Untersuchungen und Tierexperimente
unsere Kenntnis über
die Eigenschaften von Nährstofffettsäuren bezüglich Gesundheit
und Erkrankung, Wachstum und Entwicklung ausgedehnt. Als jüngstes Ergebnis
dieser Untersuchungen liegt das Augenmerk auf dem Verhältnis der ω-6/ω-3-Fettsäuren in
der Nahrung; der Essentialität
der ω-3-Fettsäuren und ihrer
metabolischen Wirkung auf die Verhinderung und Vorbeugung von chronischen
Erkrankungen. Diese biologischen und funktionellen Wirkungen der ω-3-Fettsäure üben deutliche
vorteilhafte metabolische Änderungen
bei der koronaren Herzerkrankung, Hypertonie, nicht-Insulin-abhängigen Diabetes
mellitus, Entzündungs- und
Autoimmunerkrankungen und möglicherweise
Krebs aus. Bezüglich
eines detaillierten Berichtes wegen der Quellen, Metabolismus, der
biologischen und funktionellen Wirkungen und der Diätaspekte
von ω-3-Fettsäuren vergleiche
z. B. "Functional Food" herausgegeben von Israel Goldberg, Chapman & Hall (1994) Kap. 16:
"Fatty Acids" von Artemis P. Simopoulos, S. 355 –392, das
hierin durch Bezugnahme eingefügt
wird.
-
Wir haben nun festgestellt, dass
eine Kombinationszusammensetzung, umfassend in Zumischung:
-
- (a) ein lipidlösliches Benzochinon, ausgewählt aus
der Gruppe, bestehend aus Coenzym Q10 (CoQ10) seiner reduzierten Form, Ubichinol-10
(CoQ10H2) oder Mischungen
davon in einer Menge, die wirksam ist, zur Erbringung einer therapeutischen
und/oder vorbeugenden und/oder Nährstoffaktivität bei einem
Menschen, der dieses benötigt;
und
- (b) zumindest eine ω-3-polyungesättigte Fettsäure oder
ein Ester davon;
in der Lage ist, die pharmakologischen/Nährstoffwirkungen
von CoQ10 und/oder CoQ10H2 zu verstärken.
-
Obwohl es weder beabsichtigt noch
notwendig ist, sich auf irgendeine theoretische Interpretaton zu verlassen,
um die oben genannten verstärkenden
Wirkungen au erklären;
treten diese anscheinend sehr wahrscheinlich aufgrund der ω-3-polyungesättigten
Säure auf,
die als bioakti ve Vehikel für
CoQ10 und/oder CoQ10H2 und Booster des intramitochondrialen Transportes
davon zu ihren Wirkungsstellen wirken.
-
Die Omega-3 polyungesättigte Säure ist
ausgewählt
aus der Gruppe, bestehend aus Eicosapentaensäure (EPA), Docosahexaensäure (DHA),
Linolensäure
(LNA) oder Mischungen davon. EPA und DHA oder Mischungen davon sind
insbesondere bevorzugt. Bevorzugte Ester von LNA, EPA oder DHA sind
Triglyceride und der Ethylester.
-
Die Zusammensetzung kann ebenfalls
gesättigte,
monoungesättigte
Omega-6 und Omega-9-Fettsäuren
oder Mischungen davon umfassen. Beispiele solcher Säuren sind
Paimitinsäure
(16 : 0), Oleinsäure
(18 : 1 ω9),
Linolsäure
(18 : 2 ω6)
und Arachidonsäure
(20 : 4 ω6)
oder Mischungen davon. Wenn eine oder mehrere dieser nicht-Omega-3-Fettsäuren vorhanden
sind, überschreitet
die Menge der oben genannten Omega-3-Fettsäuren, insbesondere EPA und/oder
DHA bevorzugt 65 Gew.% und ist niedriger als 95 Gew.% der Gesamtmischung
von Omega-3-Fettsäuren.
-
Das Gewichtsverhältnis von DHA : EPA in der
Zusammensetzung liegt im Bereich von 1 : 1 bis 1 : 20, bevorzugt
1 : 1 bis 1 : 5.
-
Das Gewichtsverhältnis (b) : (a) in der Zusammensetzung
liegt im Bereich von 1 : 20 bis 1 : 50.
-
Die Zusammensetzung zur Verwendung
in dieser Erfindung kann weiterhin α-Tocopherol (Vitamin E) als
Komponente (c) enthalten. Bevorzugt ist das Gewichtsverhältnis (b)
: (c) in der Zusammensetzung im Bereich von 1 : 20 bis 1 : 50. Wir
haben festgestellt, dass die genannten Omega-3-Fettsäuren als
bioaktive Vehikel gegenüber
Vitamin E ebenso agieren, d. h. dass sie die pharniakologischen
Wirkungen von Vitamin E verstärken.
-
Die Wirksamkeit der erfindungsgemäßen Zusammensetzungen
gegenüber
vielen Formen von Mitochondriopathien und die Fähigkeit der gleichen Zusammensetzungen
zur Verstärkung
des intramitochondrialen Transportes von CoQ10 wurde in klinischen
Versuchen gezeigt. Wie bei der erfolgreichen Behandlung einer Mitochondriopathie
wird über
eine Studie bei Patienten, die durch Photophobie und ARMD beeinträchtigt waren,
nachfolgend berichtet.
-
Das folgende Retinalmodell wurde
für die
Untersuchung der Mitochondriopathie verwendet.
-
Es ist bekannt, dass die reaktiven
Sauerstoffspecies (ROS) zumindest an drei Stellen in der Retina gebildet
werden kann:
-
- – in
der Photorezeptorstelle während
der Lichtstimulierung
- – in
dem retinalpigmentierten Epithelium (RPE), das Photorezeptorscheiben
während
des normalen Turnovers und der Lichtstimulierung phagozitiert;
- – in
der Neuroretina bei den Synaptosomen.
-
Bei jeder dieser drei Stellen sind
die Mitochondrien die gemeinsame Quelle und das Ziel von ROS.
-
Wir haben festgestellt, dass bei
der normalen Retina die mitochondrialen Membranen der Photorezeptorzellen
signifikant unterschiedliche molekulare Strukturen als bei den äußeren Segmentscheiben
aufweisen. Die mitochondrialen Membranen sind mehr basophil und
sie enthalten mehr ungesättigte
Lipide als die Scheibenmembranen der äußeren Pigmente. Weiterhin zeigten
in vitro Studien von normalen menschlichen Photorezeptorzellen,
dass das Verhalten der mitochondrialen und Scheibenmembranen verschieden
ist, wenn sie einer oxidoreduktiven Beanspruchung ausgesetzt werden.
Die gleiche oxidative Beanspruchung, die zu einer reversiblen Änderung
der Scheibenmembranen rführte,
verursachte eine irreversible Schädigung der mitochondrialen
Membranen. Das Aussetzen einer starken Elektronendonorsubstanz (Chlorpromazine) änderte die
Struktur der mitochondrialen Membranen etwas, aber trennte die Scheibenmembranen
auf dosisabhängige Art.
Diese Feststellung legt nahe, dass die mitochondrialen Membranen
gegenüber
oxidativer Einflüsse
sensibler sind, während
Scheibenmembranen sensibler auf reduktive Einflüsse reagieren.
-
Über
elektronenmikroskopische Studien bei erkrankten menschlichen Retinas
haben wir gezeigt, dass die mitochondriale Schädigung eine typische Änderung
der altersabhängigen
makularen Degeneration (ARMD), myopischen retinalen Dystrophien
(MRD) und bei Retinitis pigmentosa (RP) ist. Mitochondriale Änderungen
umfassten den Verlust der Kristae, die Akkumulierung von intramitochondrialen
Lipidtröpfchen,
das Quellen der Mitochondrien und die Verminderung der Zahl von
diesen wurde bei erkrankten RPE und Photorezeptorzellen beobachtet.
Pigmentepithelialzellen waren hauptsächlich bei ARMD und MRD beeinträchtigt, während bei
RP sowohl die Fotorezeptor- als auch pigmentierten Epithelialzellen
ernsthaft geändert
wurden.
-
Diese Feststellungen legten nahe,
dass die Retina ein geeignetes Modell für die Untersuchung der Mitochondriopathie
ist.
-
Wir führten offene, kontrollierte
Studien der verschiedenen Zusammensetzungen von CoQl0 und α-Tocopherol
mit oder ohne Zugabe von Omega-3- Fettsäuren durch.
In jeder Serie von gesunden Freiwilligen oder Photophobie-Patienten
wurde die Behandlung für
einen Monat durchgeführt,
während
bei der Serie der ARMD-Patienten dies für 3 Monate erfolgte. Zur Auswertung
der visuellen Funktion vor und nach der Behandlung ebenso wie einen
Monat nach dem "Auswaschen" wurde der makulare Photobeanspruchungsversuch durchgeführt.
-
Makularer Photobeanspruchungsversuch:
60 Sekunden Beleuchtung mit hellem Licht auf ein Auge (das andere
Auge wurde abgedeckt) durch eine standardisierte Schlitzlampe (volle Öffnung und
maximale Intensität
einer Haag-Streit-Schlitzlampe). Die Kontrastsensibilität wurde
das Maffei-Dezimaldiagramm
vor und nach der Bestrahlung untersucht und die Wiedergewinnungszeit
wurde gemessen (d. h. die Zeit wurde gemessen, wenn das Auge in
der Lage war, die gleiche Zahl wie vor der Fotobeanspruchung zu
lesen.
-
Diese Funktion der Retina hängt von
dem metabolischen Träger
gegenüber
der Lichtstimulations-Regeneration ab, und ist somit ein sehr geeignetes
Verfahren zur Auswertung der mitochondrialen Funktionen (Wu, G.,
Weiter, J. J., Santos, S., Ginsburg, L., Villalobos, R.: The macular
photostress test in diabetic retinopathy and age-related macular
degeneration. Arch. Ophthalmol., 108, 1556–58 (1990).
-
Die Blutgehalte des Gesamt-, HDL-
und LDL-Cholesterins und die Triglyceridgehalte wurden vor und 3
Monaten nach der Behandlung und nach einem Monat "Auswaschen" in
der ARMD-Gruppe ausgewertet.
-
a) Gesunde Freiwillige
-
12 gesunde Freiwillige wurden bei
diesem klinischen Versuch einbezogen (6 Männer, 6 Frauen, Alter 24 bis
37 Jahre, mittleres Körpergewicht:
66,5 kg).
| 1.
Gruppe: | behandelt
mit 50 mg granuliertem CoQ10 + 70 mg Vitamin
E/pro Tag |
| 2.
Gruppe: | behandelt
mit 100 mg granuliertem CoQ10 + 70 mg Vita
min E/Tag |
| 3.
Gruppe: | behandelt
mit 30 mg CoQ10 in Sojabohnenöl + 30,
mg Vitamin E/Tag |
| 4.
Gruppe: | behandelt
mit 30 mg CoQ10 in Omega-3 (>65% konz.) + 30 mg
Vitamin E/Tag |
-
Ergebnisse:
-
- – Gesunde
Freiwillige reagieren sehr schlecht auf diese Behandlungen
- – die
pharmakologische Wirkung von 50 mg granuliertem CoQ10 +
Vitamin E war unbedeutend
- – die
Lipidzugabe verbesserte die Dosis-Wirkungsbeziehung von CoQ10 + Vitamin E (100 mg granuliertes CoQ10 waren äquivalent
zu 30 mg CoQ10 das in Sojabohnenöl aufgelöst worden
war)
- – hoch
konzentriertes PUFA war die effektivste Behandlung.
-
b) Photophobie-Patienten
-
16 Patienten litten an Photophobie
und wurden bei diesem Versuch einbezogen (11 Frauen, 5 Männer, Alter
23 bis 44 Jahre, mittleres Körpergewicht
63,4 kg).
| 1.
Gruppe: | behandelt
mit 100 mg granuliertem CoQ10 + 70 mg Vitamin
E/Tag |
| 2.
Gruppe: | behandelt
mit 30 mg CoQ10 in Sojabohnenöl + 30 mg
Vitamin E/Tag |
| 3:
Gruppe: | behandelt
mit 30 mg CoQ10 in Fischöl (>30% Konzentration) + 30 mg Vitamin E/Tag |
| 4.
Gruppe: | behandelt
mit 30 mg CoQ10 in Omega-3 (>65% Konz.) 30 mg Vitamin
E/Tag |
-
Ergebnisse
-
Die pharmakologische Wirkung von
CoQ10 + Vitamin E war ungefähr doppelt
so hoch bei der Photophobie wie bei gesunden Freiwilligen.
-
- – Omega-3
verstärkte
die Intensität
und Dauer der pharmakologischen Wirkungen von CoQ10 +
Vitamin E;
- – eine
höhere
Konzentration von Omega-3 zeigte bessere Wirkungen als eine niedrige
Konzentration: die Unterschiede waren 50% nach einmonatiger der
Behandlung und ungefähr
30% nach einem Monat "Auswaschen".
-
c) Retinaldystrophie-Patienten
-
43 Patienten, die durch die frühe altersbezogene
makulare Degeneration (Sehschärfe
besser als 20/40) beeinträchtigt
waren, waren bei diesen Studien involviert (23 Frauen, 20 Männer, alter
zwischen 55 und 66 Jahren, mittleres Körpergewicht 66,8 kg)
| 1.
Gruppe: | behandelt
mit Lutein + Zeaxantin + Vitamin E (kommerzieller hältliches
Produkt) |
| 2.
Gruppe: | nur
mit 1000 mg Omega-3 (> 65%)
behandelt |
| 3.
Gruppe | behandelt
mit Fischöl
+ 30 mg CoQ10 + 30 mg Vitamin E/Tag |
| 4.
Gruppe: | behandelt
mit Omega-3 (>65%)
+ 30 mg CoQ10 + 30 mg Vitamin E/Tag |
-
Ergebnisse
-
Es gab keine signifikanten Ergebnisse
zwischen den Gruppen, die mit einer kommerziell erhältlichen Diätergänzung (umfassend
Lutein, Zeaxantin und Vitamin E) und Omega-3 (>65%) alleine behandelt wurden.
-
- – CoQ10 + Vitamin E in hoch konzentriertem Omega-3
war effektiver als Fischöl
+ CoQ10 + Vitamin E nach 3 Monaten (50%)
und nach einem Monat Auswaschen (30%);
- – hoch
konzentriertes (>65%)
PUFA zeigte synergistische pharmakologiche Wirkungen mit CoQ10 und
Vitamin E, die besser waren als solche mit einer niedrigen Konzentration
an PUFA oder gesättigten
Lipiden;
- – hoch
konzentrierte (>65%)
PUFA-Verabreichung zeigte die Erniedrigung der Plasmatriglyceridgehalte und
verbesserte das Verhältnis
des Gesamt/HDL-Cholesterins, was bei den mit Fischöl (30% Omega-3)
behandelten Fällen
nicht beobachtet wurde. Im Gegensatz wurde bei 3 der 12 Fälle eine
Zunahme des Gesamtcholesterins und/oder Triglyceridgehalt beobachtet.
-
Tabelle
I Gesunde Freiwillige
-
Tabelle
II Photophobie-Patienten
-
Tabelle
III Altersbezogene makulare Degeneration
-
Ergebnisse
-
Diese pharmakologischen Untersuchungen
zeigten, dass CoQ10 + Vitamin E in einem
Vehikel aus hoch konzentrierten polyungesättigten Fettsäuren die
Retinalfunktion, hauptsächlich
die Regeneration der Photorezep torzellen im normalen Zustand und
bei den Erkrankungszuständen
verbesserten.
-
Das wahrscheinlichste zelluläre Ziel
dieser Substanzen sind die Mitochondrien der Fotorezeptorzellen. Die
längere
Dauer der visuellen Verbesserung, eine besonders wichtige pharmakologische
Wirkung zeigt an, dass die Zusammensetzung dieser Erfindung eine
höhere
intrazelluläre
Konzentration von CoQ10 und/oder höhere Affinität dieser
Substanz für
die Zielorganellen erreicht als solche, die über die üblichen enteral verabreichbaren
CoQ10 haltigen Formulierungen, die gegenwärtig kommerziell
erhältlich
sind, erzielt werden können.
-
Die folgenden Beispiele der Zusammensetzungen
werden zur Erläuterung
und nicht zur Beschränkung
angegeben. Beispiel
1: 700 m (*) weiche Gelatinekapseln
| Eicosapentaensäure (EPA) | 148,72 mg |
| Docosahexaensäure (DHA) | 105,82 mg |
| Linolensäure (LAN) | 31,46 mg |
| Coenzym
Q10 | 10,00 mg |
| Proteine | 137,00 mg |
| Kohlenhydrate | 63,00 mg |
Beispiel
2: 1420 mg (*) weiche Gelatinekapseln
| Eicosapentaensäure (EPA) | 340 mg |
| Docosahexaensäure (DHA) | 240 mg |
| Linolensäure (LAN) | 70 mg |
| Coenzym
Q10 | 20 mg |
| Vitamin
E | 20 mg |
| Proteine | 300 mg |
| Kohlenhydrate | 150 mg |